Почему окислительная способность элементов 6 группы главной подгруппы

Лекция №12. Периодическая система элементов. s – элементы.
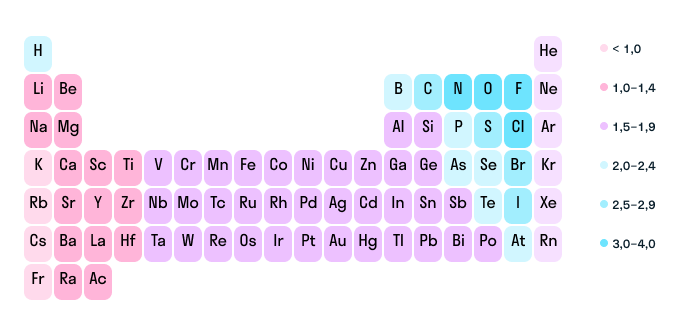
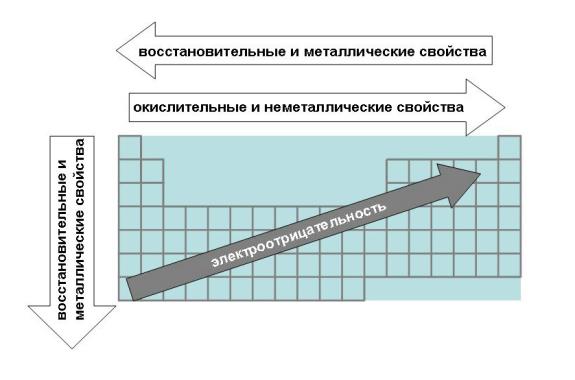
К р-элементам VI группы периодичесrой системы элементов Д. Менделеева относятся кислород, сера, селен, теллур и полоний. Кислород и сера являются типическими элементами; селен, теллур и полоний образуют семейство селена. В ряду :. Энергия сродства к электрону, энергия ионозации, электроотрицательность уменьшаются. Н еметаллические свойства и окислительная способность уменьшаются.







В химии степень окисления элементов говорит о том, как проходят окислительно-восстановительные реакции, а точнее — как при этом атомы перераспределяют между собой электроны. Это не очень сложная тема, но в ней часто бывает путаница. Разберемся, как считать степень окисления в разных соединениях. Для начала давайте вспомним, как проходят химические связи в молекуле вещества.










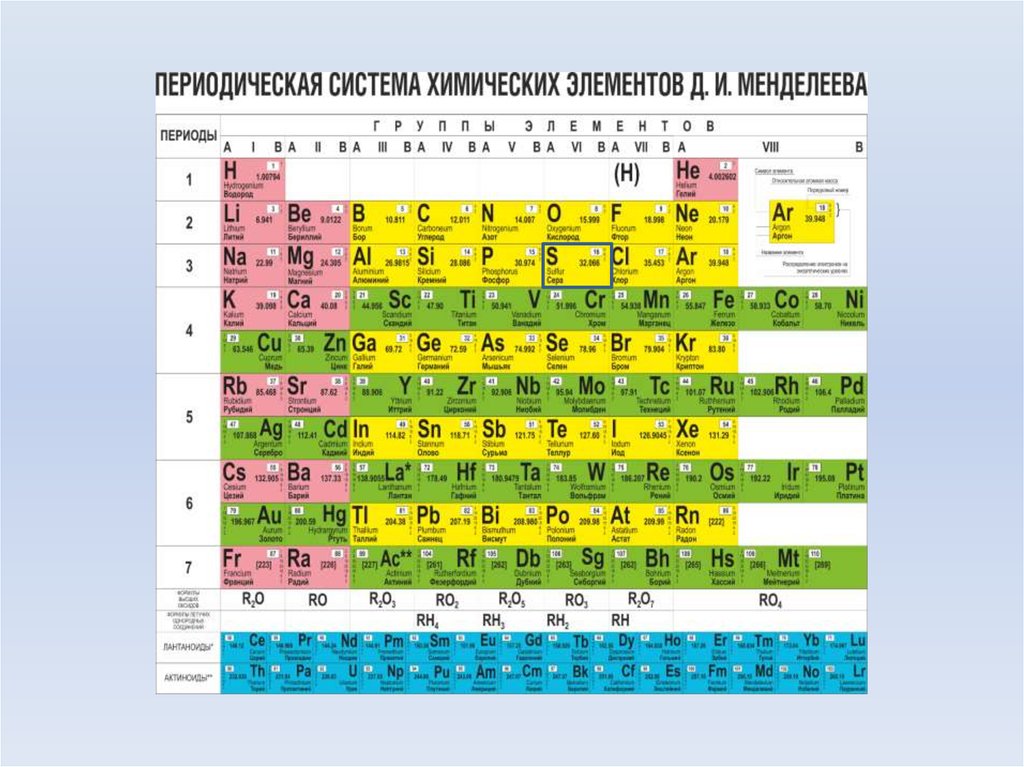


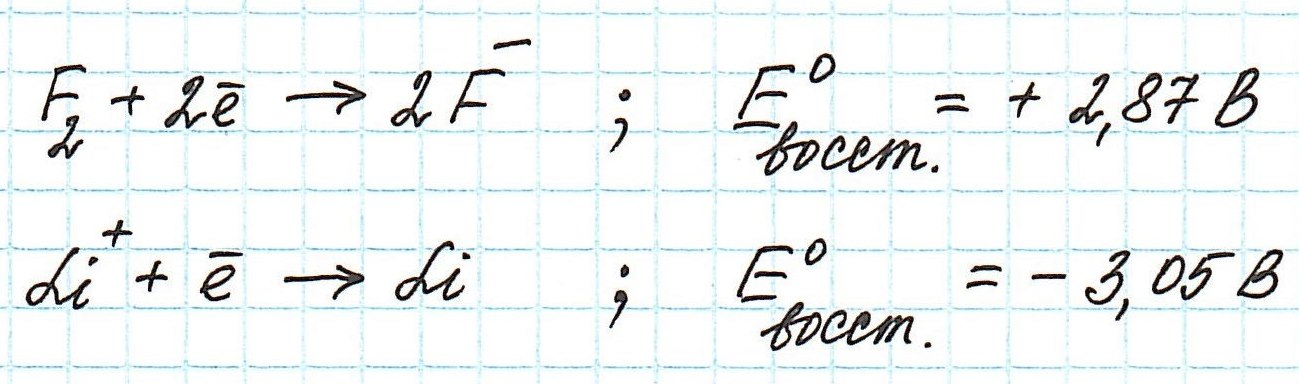
Менделеева по устаревшей классификации — элементы главной подгруппы VII группы [1]. Реагируют почти со всеми простыми веществами, кроме некоторых неметаллов. Все галогены — энергичные окислители , поэтому встречаются в природе только в виде соединений.









